Da Redação
O câncer de pâncreas é um dos mais agressivos e apresenta uma alta taxa de mortalidade em cinco anos. Estima-se que apenas cerca 20% dos casos são diagnosticados no estágio inicial e, desta forma, passíveis de cirurgia. Felizmente, a chegada de um novo tratamento no país traz esperança de que mais pessoas possam ter melhores expectativas de sobrevida. O intervencionista oncológico Luiz Tenório Siqueira e o cirurgião Antônio Luiz Macedo realizaram neste domingo (28), no hospital Vila Nova Star, em São Paulo, o primeiro procedimento de eletroporação irreversível com a Nanoknife para tratar um câncer de pâncreas. A incorporação da nova tecnologia oferece melhores perspectivas, principalmente aos pacientes que já apresentam o tumor em estado localmente avançado.
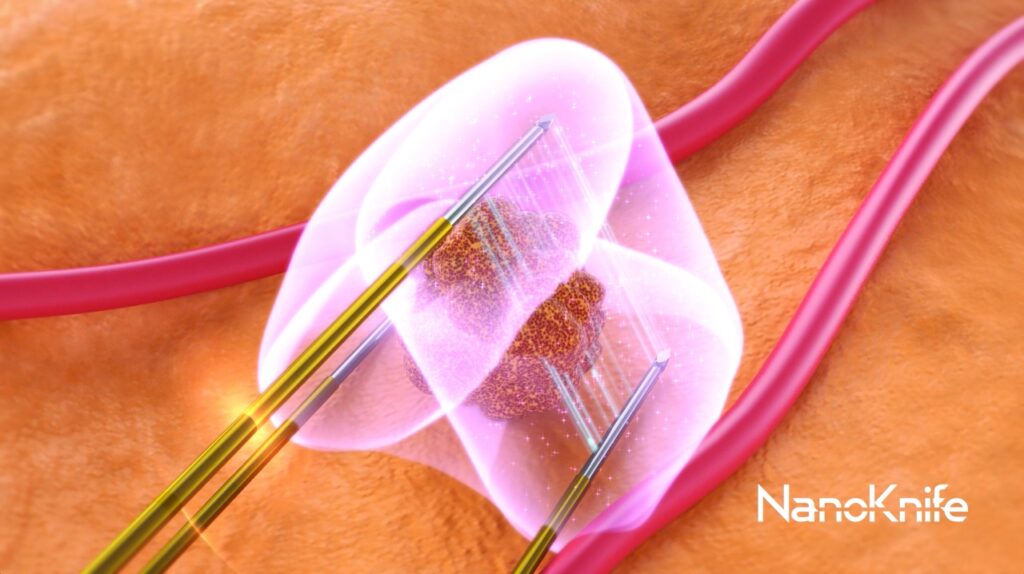
“Essa tecnologia inédita no país usa agulhas para dar choques de alta voltagem no tumor, matando as células cancerígenas. Com esse esforço da Rede D’Or, trazendo esse novo equipamento, pacientes com câncer de pâncreas ganham uma nova alternativa nesse tratamento tão difícil”, explica Tenório.
No caso do câncer de pâncreas, a falta de sintomas na fase inicial resulta, na maioria dos casos, em diagnóstico tardio, o que reduz ainda mais a chance de cura. “Até então, a ressecção de tumores que invadiam importantes artérias do abdome era difícil ou mesmo impossível de ser realizada. E, geralmente, a expectativa de vida desse paciente é baixa. Agora, podemos melhorar esse cenário”, observa o radiologista.
É esse o caso da primeira paciente. Claudia Maria Meirelles, de 55 anos, que há seis meses vem realizando rádio e quimioterapia neoadjuvantes, mas que talvez não conseguisse ressecar completamente o tumor sem esse avanço tecnológico. “Seria muito difícil ser operado e ter margens livres de tumor sem a Nanoknife”, afirma Tenório, que explica que os tratamentos cirúrgicos anteriores, além de oferecerem maior risco à vida do paciente, pois havia chance de afetar estruturas vitais, como vasos que nutrem o fígado e intestino, poderiam não retirar o tumor completamente. “Agora temos um procedimento cirúrgico mais seguro, menos invasivo e com maior chance de sucesso oncológico. “Dependendo do caso, não é preciso abrir a barriga, pôde-se fazer guiado por imagem de forma minimamente invasiva e o paciente recebe alta no dia seguinte”, conta.
Ele ainda explica que o equipamento utiliza uma técnica de ablação moderna. São usados eletrodos paralelos, posicionados lateralmente ao tumor que, quando aplicada uma tensão definida, transferem a ondas de alta voltagem de um lado para o outro, criando nanoporos permanentes na membrana celular, interrompendo a homeostase, criando um efeito que leva à morte a célula cancerígena.
“A ablação já era utilizada para combater outros cânceres, como pulmão, rins e fígado. Entretanto, as tecnologias predecessoras não permitiam o uso em tumor de pâncreas, pois geravam calor ou frio, o que machucava os órgãos e vasos ao redor do pâncreas. A Nanoknife não altera a temperatura, o que permite a realização em tumores de pâncreas”, esclarece.
Câncer de pâncreas em números
De acordo com dados do Instituto Nacional de Câncer (Inca), o câncer de pâncreas é responsável por cerca de 2% de todos os tipos de câncer diagnosticados e por 4% do total de mortes causadas pela doença. Por ano, mais de 11 mil pessoas morrem no país devido à doença. Raro antes dos 30 anos, torna-se mais comum a partir dos 60 e tem maior incidência entre os homens.





